INTEGRAZIONE
DI SCIENZA, CLINICA E SANITA’
Nuova
opportunità per la farmacologia clinica italiana?
Diventa
sempre più impegnativo illustrare ai nuovi ricercatori quali siano i compiti di
un farmacologo e le differenze tra i diversi settori della farmacologia.
Nella
ricerca farmaceutica, tradizionalmente il farmacologo è il ricercatore che
studia l’attività dei composti su modelli in vivo ed in vitro, mentre il
farmacologo clinico studia generalmente gli effetti dei nuovi composti nel
volontario sano o in popolazioni selezionate di pazienti. Il ricercatore che
coordina sperimentazioni cliniche di solito non viene considerato o percepito
come farmacologo, diversamente da quanto avviene in ambito accademico, dove
nella definizione di farmacologia clinica rientrano tutte le diverse attività
condotte sul soggetto umano, dal monitoraggio delle concentrazioni ematiche dei
farmaci fino alla ricerca farmacoepidemiologica.
Questo
scenario è destinato a cambiare rapidamente ed e in parte gia superato. Spinta
dalla innovazione tecnologica e dalla evoluzione sanitaria, la farmacologia
clinica è entrata in una fase di rapida, intensa e talora confusa
trasformazione, che – incurante di distinzioni e definizioni – modificherà
i tradizionali assetti, ruoli ed equilibri sui quali e vissuta per decenni.
Stanno
cambiando rapidamente e radicalmente le modalità con le quali il farmaco viene
scoperto, sviluppato, sperimentato, illustrato, prescritto, utilizzato,
rimborsato e le ragioni di questo cambiamento vanno ricercate soprattutto nei
nuovi orizzonti della scienza, della clinica e della sanità.
Scienza
La
tecnologia informatica e le applicazioni della genomica hanno iniziato a
rivoluzionare il processo di scoperta dei nuovi farmaci. Le cause principali del
fallimento di molti progetti di drug discovery sono tuttora rappresentate dalla
imprecisa selezione del target (e quindi i target molecolari non sono rilevanti
per la malattia) o del composto candidato allo sviluppo (e quindi i composti che
non hanno le proprietà per essere dei farmaci oppure che non rappresentano le
molecole migliori).
Nel
loro complesso, l’insieme dei farmaci attualmente in uso ed in corso di
sviluppo interagisce con poco più di 500 target (enzimi, recettori, canali
ionici ecc.); a seguito della conclusione del progetto Genoma Umano nel 2003 e
dello sviluppo della genomica funzionale, tra dieci anni i target da selezionare
per la scoperta di nuovi composti potranno essere oltre 18.000.
Nei
prossimi decenni la conoscenza dei geni, della loro localizzazione, dei loro
prodotti e delle modalità con cui interagiscono tra loro nel processo
patologico rappresenterà probabilmente la principale, se non l’unica modalità
di identificazione di nuovi target per la scoperta del farmaco.
Oltre
alla possibilità di migliorare la selezione dei target, sta aumentando
enormemente anche la capacità di sintetizzare nuove molecole e di testarle in
modo rapido ed efficiente contro i diversi target. Rivoluzionando il vecchio
paradigma di una molecola, un chimico, una settimana, la tecnologia ora consente
ad un solo chimico che utilizza computer e robot, di sintetizzare centinaia di
migliaia di nuove molecole, creando una diversità di composti impensabile fino
a pochi anni fa.
Per
valutare in modo efficiente questo enorme numero di nuove molecole, sono stati
sviluppati e sono già in uso sistemi di high throughput screening ed altri
metodi predittivi che permettono di rilevare eventuali interazioni dei composti
in screening con i target in esame oppure di generare, utilizzando un solo
animale, dati di farmacocinetica su 100 molecole in un solo giorno, migliorando
sensibilmente la resa rispetto al passato, quando per ottenere dati su un solo
composto erano necessari sei animali ed una settimana di lavoro.
Rispetto
alla farmacologia tradizionale, che operava in laboratorio con test in vitro ed
in vivo, siamo già entrati in quella che taluni hanno definito farmacologia di
terza generazione o in silico, che vede nella tecnologia ed in particolare nella
genomica e nella bioinformatica i principali strumenti di lavoro del farmacologo
[1].
Tabella
1. Anni per arrivare all’80% delle applicazioni commerciali derivanti dalle
nuove tecnologie di ricerca e sviluppo dei farmaci
|
Chimica combinatoriale Ultra High Throughput Screening Genomica Bio-informatica Farmacogenomica Virtual Drug Discovery Terapia Genica |
2 4 5-7 3 7-8 7-9 10-15 |
(Morgan Stanley Dean Witter, 1998)
Clinica
Il
significato di farmacologo clinico varia a seconda dei contesti ai quali viene
riferito e nella ricerca dell’industria farmaceutica, indica l’esperto della
valutazione dei nuovi composti sperimentali nel soggetto umano, sano o paziente,
nelle fasi iniziali di sviluppo clinico, della loro cinetica e dello studio del
meccanismo d’azione mediante modelli sperimentali sul soggetto umano.
La
valutazione iniziale dei nuovi composti nel corso delle prime somministrazioni a
soggetti umani è una attività che in Italia rischia di diventare un ricordo più
che una esigenza professionale. Nel nostro paese infatti una limitata capacità
di scoperta di nuovi farmaci ed una serie di difficoltà normative hanno in
pratica limitato il ruolo della farmacologia clinica ad occasionali studi di
bioequivalenza e biodisponibilità. Difficoltà ancora maggiori sembrano
interessare lo studio dei meccanismi d’azione in modelli sperimentali su
volontari sani e pazienti: assimilato nella nostra normativa alla prima
somministrazione di un nuovo composto, rischia di essere escluso da reali
possibilità applicative.
La
farmacologia clinica e (o almeno, dovrebbe essere) la piattaforma metodologica
di tutta la sperimentazione clinica, indipendentemente dalla area terapeutica di
interesse. II DM 18 marzo 1998 sulla composizione dei Comitati Etici ha almeno
in parte ripreso questo concetto, riconoscendo al farmacologo il compito di
garanzia metodologica della sperimentazione clinica.
Il
contributo del farmacologo alla sperimentazione clinica ed al suo sviluppo in
Italia è rimasto tuttavia modesto, se non trascurabile.
La
gestione delle procedure di autorizzazione, sia a livello centrale che locale,
ha emarginato fino a non molti mesi fa il nostro paese dallo sviluppo
internazionale dei nuovi farmaci: sono state purtroppo ben poche le iniziative
tese a segnalarne le conseguenze per la ricerca italiana, per modificare la
situazione nei tempi più rapidi possibili e per evidenziare il ruolo della
sperimentazione clinica del farmaco nello sviluppo del sistema di ricerca
nazionale.
Risolta
l’emergenza con i decreti del 1998, sono riemersi i problemi che ostacolano il
reale sviluppo della ricerca clinica farmacologica nel nostro paese ed in
particolare l’impossibilita di realizzare ricerca clinica per le patologie
gestite sul territorio e la difficoltà, quasi impossibilità, di proseguire lo
sviluppo del farmaco dopo la sua commercializzazione, nella fase 4.
In
Italia l’accesso alla sperimentazione clinica è limitato esclusivamente ai
pazienti degenti in strutture ospedaliere oppure assistiti presso gli ambulatori
divisionali. Ciò esclude una rilevante proporzione di cittadini dalla
possibilità di partecipare alla sperimentazione clinica di farmaci per
patologie di rilevante interesse e limita la rappresentatività di altre
patologie che vengono trattare in ambiente ospedaliero.
Farmaci
antivirali per il trattamento della influenza o della varicella, farmaci per il
trattamento della sindrome del colon irritabile – solo per citare alcuni dei
problemi di salute che non hanno ancora trovato una adeguata soluzione
terapeutica – possono essere sperimentati in modo efficiente solo negli
ambulatori dove il paziente si reca per ricevere assistenza e terapia. Ad
esclusione di Italia, Panama, Taiwan, Corea del Sud e pochissimi altri paesi, in
tutto il resto del mondo la collaborazione tra farmacologia (che assicura le
necessarie competenze di metodologia e la formazione specifica), medicina
specialistica universitaria od ospedaliera (che fornisce le competenze per
standardizzare le diagnosi o le valutazioni delle risposte terapeutiche) e
medicina del territorio (medicina generale e pediatria di libera scelta)
consente di sviluppare la maggior parte dei farmaci che poi saranno utilizzati
nella pratica assistenziale [2].
Come
conseguenza di questa situazione, il numero di pazienti potenzialmente
eleggibili per la sperimentazione clinica di molte malattie croniche risulta in
Italia alquanto limitato e quindi il contributo italiano allo sviluppo clinico
internazionale dei nuovi farmaci è inferiore a quello di paesi come Olanda,
Svezia, Spagna, paesi con popolazioni di gran lunga inferiori.
Questi
limiti regolatori e normativi appariranno ancora più evidenti ed acuti quando
le applicazioni della genomica avranno rivoluzionato le modalità di sviluppo
clinico e di utilizzo del farmaco, ovvero con lo sviluppo della farmacogenomica.
La
maggior parte dei farmaci sottoposti a sperimentazione clinica presenta
percentuali di risultati positivi limitati al 50%-60%, in quanto solo una parte
dei pazienti è realmente appropriata per il farmaco oggetto della
sperimentazione, mentre gli altri – anche se appaiono simili per quanto
riguarda il fenotipo – non sono idonei dal punto di vista del genotipo.
Gli
attuali criteri di inclusione ed esclusione per la selezione dei pazienti nella
sperimentazione clinica (criteri di inclusione ed esclusione) considerano
infatti solo il fenotipo del paziente: sono tuttavia sempre più numerose le
sperimentazioni cliniche nelle quali viene praticata la tipizzazione genetica
per poter identificare i geni correlati con la predisposizione alla malattia, la
risposta terapeutica, le eventuali reazioni avverse e le caratteristiche
cinetiche dei nuovi farmaci.
Disponendo
dell’informazione sul genotipo del paziente e sulla risposta terapeutica del
farmaco (o di farmaci con simile meccanismo di azione) nella popolazione di
pazienti genotipicamente omogenea, risulterà assai più facile selezionare i
pazienti per la sperimentazione clinica e ridurre il numero necessario per
provare le ipotesi sperimentali, con evidenti implicazioni sui tempi di
sviluppo, sui costi e sulla qualità dello sviluppo.
La
rilevanza delle informazioni acquisite attraverso la farmacogenomica va ben
oltre l’ambito della sperimentazione clinica: la possibilità di prescrivere
il giusto farmaco per il giusto paziente, sulla base del genotipo, permetterà
di ottimizzare la risposta terapeutica, limitando il trattamento ai solo
pazienti idonei, di prevenire eventuali reazioni avverse e nel complesso di
migliorare l’efficienza del processo assistenziale [3].

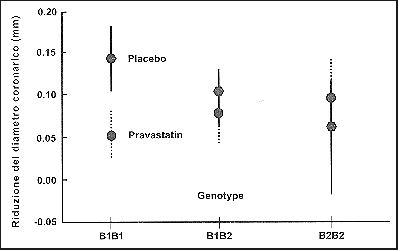
Figura
1. Relazione tra genotipo CEPT (cholesteryl
ester transfer protein), progressione della aterosclerosi (misurata
mediante riduzione del diametro coronarico) ed efficacia della terapia
con pravastatina (da Kuivenhoven et al., 1998, New Vngl. J. Med 338 86-93).
Sanità
In
tutto il mondo occidentale l’evoluzione della sanità interessa tutti i
settori della società e rappresenta uno dei principali argomenti nelle agende
politiche ed istituzionali. Proprio in questi giorni sono in corso dibattiti nel
Regno Unito [4] sulla istituzione del National Institute of Clinical Excellence
(NICE), una istituzione attivata dall’aprile del 1999 per fornire indicazioni
sulla effectiveness e sulla convenienza economica delle tecnologie sanitarie (la
cui direzione e stata peraltro affidata ad un farmacologo clinico, Michael
Rawlins) ed in Italia sul nuovo decreto legislativo sulla razionalizzazione del
servizio sanitario.
Molte
delle terapie di maggiore e documentata efficacia attualmente disponibili sono
basate sul farmaco, che consente di realizzare interventi sanitari di importanza
primaria per la soluzione dei problemi di salute.
E’
pertanto del tutto comprensibile che molti degli interventi sulla sanità
interessino anche il farmaco. Come in altri settori, è importante che le
decisioni siano prese sulla base di informazioni e che la valutazione della
qualità, della efficacia e della appropriatezza degli interventi avvenga sulla
base di prove documentate.
La
ricerca sul farmaco, inteso quale tecnologia sanitaria, rappresenta un aspetto
primario della ricerca sanitaria e la farmacoepidemiologia rappresenta una
piattaforma metodologica fondamentale per la realizzazione di progetti che
misurino i bisogni di assistenza sanitaria delle popolazioni e valutino la
qualità della assistenza erogata [5].
A
parte alcune eccezioni, frutto più di iniziative personali ed occasionali di
alcuni centri di eccellenza che di una volontà programmata e coordinata, la
farmacologia è rimasta sostanzialmente ai margini della ricerca sanitaria. La
documentazione sul valore del farmaco richiede l’integrazione di informazioni
di farmacologia preclinica e clinica con informazioni farmacoepidemiologiche e
sanitarie e la rilevanza di queste ultime diventa sempre più importante per le
decisioni sul rimborso del farmaco, sulla inclusione nei prontuari terapeutici,
sulla appropriatezza dei processi prescrittivi, per la definizione di linee
guida e percorsi terapeutici.
Il
dibattito sull’informazione sul farmaco, attualmente in corso sia in ambito
internazionale [6] che nazionale, interessa il ruolo del paziente quale soggetto
attivo nella decisione terapeutica, l’utilizzo di nuove modalità di
comunicazione quali il Direct-to-Customer, autorizzato dalla FDA nel 1997 e di
nuovi supporti tecnologici, l’ambito di intervento e di controllo delle
autorità regolatorie. Questo dibattito ha finora visto un intervento
sostanzialmente marginale della farmacologia italiana, che al contrario può
avere un ruolo primario nell’uso razionale dei farmaci e nell’educazione
della classe medica per l’ottimale utilizzazione dei farmaci.
Conclusioni
Scienza,
clinica e sanità rappresentano tre nodi di un flusso continuo ed ideale di
dati, informazioni e conoscenze sul farmaco, nel quale la scienza interagisce
con la clinica, la clinica con la sanità e questa ultima con entrambe.
Dove
si colloca la farmacologia italiana, intesa nel senso più ampio di patrimonio
collettivo di conoscenze di quanti ricercano, sviluppano e studiano il farmaco?
Probabilmente non esiste una sola risposta e le risposte possono variare a
seconda della prospettiva di valutazione. Tuttavia, se si considera quanto è
stato sopra sottolineato, sembra che molti dei grandi temi che interessano
scienza, clinica, sanità e quindi ricerca, sviluppo ed impiego del farmaco,
siano oggi trattati in Italia senza un contributo significativo della farmacologia clinica italiana.
Esistono
diversi progetti, taluni di notevole rilevanza ed interesse, ma si tratta di
iniziative di singoli farmacologi più che della farmacologia.
Vi
sono oggi opportunità e possibilità perché la farmacologia possa sviluppare
il proprio ruolo ed intervenire in settori fino ad oggi scarsamente presidiati.
I
nuovi scenari della scienza, della clinica e della sanità offrono alla
farmacologia clinica italiana uno spettro di potenziali attività, iniziative e
progetti senza precedenti, ma richiede un adeguamento delle proprie conoscenze e
dei propri metodi di lavoro altrettanto impegnativo ed una volontà
organizzativa che tenda a superare i limiti delle definizioni e delle differenze
per essere in grado di presidiare fenomeni in rapida e continua evoluzione.
Come
ogni medaglia, questi scenari contengono anche rischi, il primo dei quali è il
rischio di obsolescenza, di compiere attività ormai largamente superate dalla
innovazione tecnologica e scientifica che ha investito la ricerca sul farmaco.
Il
secondo rischio, altrettanto reale, riguarda la competizione: se la farmacologia
non entra in modo deciso e con competenza in questi nuovi settori della scienza
e soprattutto della clinica e della sanità, altri vi entreranno e ne gestiranno
attività e contenuti. Le modalità per cogliere queste opportunità riguardano
aspetti di tipo metodologico ed organizzativo; c’è un solo problema: il
tempo. Evoluzioni, rivoluzioni e cambiamenti progrediscono con il proprio passo.
Poche settimane fa, in un auditorium desolatamente deserto, veniva presentato il
rapporto su Ricerca e Sviluppo ed industria farmaceutica italiana: le sfide per
il futuro, le cui conclusioni riassumono in modo esemplare l’intero problema:
La
storia recente dell’Italia è purtroppo ricca di sconfitte nelle sfide
competitive globali. Solo se si abbandona un approccio individualistico e si
incomincia a ragionare in termini di progetti congiunti si può vincere
la sfida. Ma i margini di manovra per quanto riguarda il tempo sono molto
serrati.
Subito
ed insieme sono le parole chiave per vincere questa sfida.
Giuseppe
Recchia
Direttore
Medico
Glaxo
Wellcome
Ricerca e Sviluppo ed
industria farmaceutica italiana: le sfide per il futuro, Centro Studi e
Ricerche di Economia Sanitria, Gemini Consulting, 1999.
Panorama della Sanità,
1999.
MH
Richmond. The implications of genetics and genomics for healthcare and the
pharmaceutical industry. University College London, London 1999.
M
Rawlins. National Health Service: in pursuit of quality, the National
Institute of Clinical Excellence. Lancet 1999; 353: 1079-82.
ASL, distretto, medico di
base: logiche e strumenti manageriali. A cura di F Longo, EGFA Edizioni
Giuridiche Economi- che Aziendali dell’Università Bocconi, Milano 1999.
6. DTC JAMA 1999.